客户服务热线
15018755050 刘老师18576633499 卢老师
常见问题解答:
1.问:如果已做过一个工艺验证,有关杂志标准为已知杂质≤0.15%,未知杂质≤0.1%,在CEP审评过程中,由于计量>2g,EDQM要求将杂质(包括已知未知)限度降低到ICH Q3A要求的≤0.05%,原来验证过的工艺能生产出50%的样品符合新的限度要求,那么,此工艺还需要再进行验证生产出100%的样品都符合杂质 ≤0.05%的要求吗?还是可以维持原来的工艺验证,挑批次符合CEP要求,其余批次符合其他市场的质量要求?答:因为是日服最大剂量,有些制剂产品的日服最大剂量在低于2克以下的话,那么,有些批次未知杂质在0.05%以上,从市场角度来说,可以销售。这是品种问题。但是从GMP角度来说,想把药品的杂质降到0.05%以下,可能涉及到最后一步引入了再次精制过程。如果是这样,这个工艺是需要全部验证的。
2.问:容易被Ⅰ类溶媒所污染的溶媒在日常使用及检测过程中应注意哪些问题,如丙酮、甲醇?
答:建立适当的限量进行控制,或者证明成品当中Ⅰ类溶媒不存在,没有检测出来。
3.问:我们再申报资料中对产品杂质A提出了不超过0.3%的限度(杂质A已经列在药典专论的杂质列表中了,而且专论对于单个杂质的限度是NMT0.5%),但是再获得的证书上并没有列出这个NMT0.5%的限度。我们想知道,0.3%和0.5%,哪个是批准的限度?我们可以把杂质A含量高于0.3%的产品作为CEP产品出售吗?
答:通常来说,在CEP证书上,如果已经出现在欧洲药典的杂质清单上的杂质,不会在CEP证书上出现。除非控制欧洲药典列出杂质的方法跟药典方法不一致,方法不同可能限度就不一样,检测的结果也不一样。在这种情况下,就会把已列出杂质列在CEP证书上。

理清认证思路


提交申报材料


建立申报文件


审核老师进场审核


证书在认监委可查
答:主要有证书编号、公司名称、公司认证规模大小(小、中、大)、业务范围、证书有效期、发证机构名称。
答:根据公司人数不同,周期会略有浮动。一般情况下,办理ISO9001质量管理体系认证需要一个月左右,二合一(9001+14001)一个半月左右,三合一(9001+14001+18001) 一个半月左右。
答:1-50人是属于小规模S,51-1000人是属于中规模M,大于1000人属于大规模L
答:证书每年需要监督审核,第三年需要复评。

所属行业:IT 获得证书:2016年08月30日
我们集团的各大认证项目基本上都是交给东方信诺去做的,长期以来,合作的非常愉快,我们也向其他家合作公司推荐了东方信诺。未来对于信息安全的要求更高,首先必须要符合国际标准,通过认证可以提升企业在同行业中的优势地位,对企业发展意义很大。

所属行业:机械 获得证书:2016年08月30日
东方信诺对项目的进度控制的很好,证书按计划顺利的拿到了。这个证书对于我们很重要,目前多投入的人力时间和金钱成本都会在日后的不断发展中转化成更大的效益。对于信息安全管理算是有个标准化的要求。

所属行业:IT 获得证书:2016年08月30日
我们公司对于信息安全管理这方面非常看重,获得国际认可的机构的认证证书,对于未来公司在洽谈和开发业务上有了更多的优势,也增强了投资者信心和服务客户的能力。在培训的过程中,东方信诺的培训老师可以说比较敬业和专业,整个认证的过程沟通很顺畅。

所属行业:IT 获得证书:2016年08月30日
常见问题解答认证,一直在我们公司的发展规划系统里,信息安全这一块越来越不容忽视,不得不说选择了东方信诺帮做这个项目是很机智的,除了拿证之外,公司的信息管理水平也得到了提升。

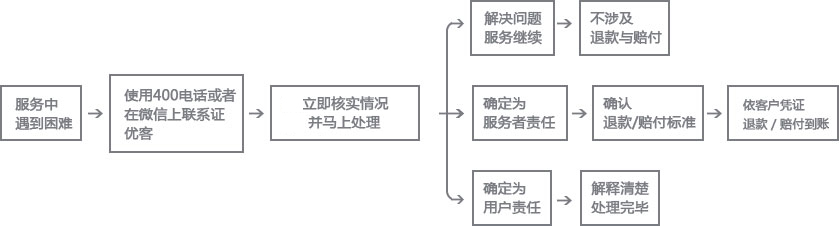
关于服务质量的反馈,我们会第一时间专人处理,保证及时解决您的问题。

1.拨打0755-32322228 ,选择投诉;
2.点击在线投诉按钮,描述详情;
3.通过微信公众号等方式,联系我们。